Brancheforeninger: EU-krav kan få markedet for diagnostiske test til at stivne

Henrik Christensen
Formand, DiaLab
Lene Laursen
Vicedirektør, Medicoindustrien
Katrina Feilberg Schouenborg
Branchedirektør, Sundhed og Life Science, Dansk Erhverv
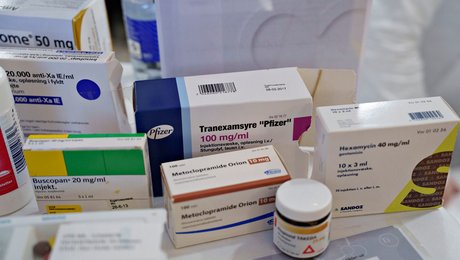
På bare få år er diagnostiske test rykket helt frem i danskernes bevidsthed. Under coronapandemiens hærgen blev det nemlig hverdag at bruge PCR- og antigentest som led i at overkomme en af de største sundhedskriser i det seneste århundrede.
Ingen kunne længere være i tvivl om, hvor vigtig diagnostik er for vores allesammens sundhed.
Men diagnostiske test handler ikke kun om at kunne teste sig ud af en coronapandemi.
De bruges på daglig basis mange andre steder i sundhedsvæsenet og er eksempelvis helt afgørende for tidlig opsporing af alvorlige sygdomme og justering af igangværende behandlinger. Derfor er det vigtigt, at det danske sundhedsvæsen altid har nem adgang til det bedste og mest innovative diagnostiske udstyr.
Ny forordning skaber flaskehalse
Desværre ser tilgængeligheden af nye diagnostiske produkter til de europæiske sundhedsvæsener, herunder også det danske, ud til at blive alvorligt udfordret inden for en forholdsvis kort tidshorisont.
I sidste uge trådte den nye EU-forordning for in vitro-diagnostisk udstyr (IVDR) i kraft på tværs af EU. Den nye forordning medfører blandt andet, at omtrent 80 procent af det diagnostisk udstyr i fremtiden vil skulle have en godkendelse mod kun otte procent i dag.
Branchen står fortsat tilbage med en stor usikkerhed i forhold til nye produkter
Henrik Christensen, Lene Laursen og Katrina Feilberg Schouenborg
Hhv. formand, DiaLab, vicedirektør, Medicoindustrien og markedschef, Dansk Erhverv
De markant skærpede godkendelseskrav til diagnostisk udstyr betyder, at der i øjeblikket er et uforholdsmæssigt stort pres på de i alt kun syv bemyndigede organer, som står for godkendelsesprocedurerne af diagnostisk udstyr på tværs af EU’s 27 medlemslande.
Det bidrager til flaskehalse, som både forsinker udbredelsen af nye produkter til markedet og risikerer at medføre, at en lang række livsnødvendige diagnostiske test vil falde helt ud, fordi de ikke kan nå at blive godkendt efter de nye regler.
Bekymringen forstærkes desuden af, at den fælleseuropæiske database for medicinsk udstyr, EUDAMED, endnu ikke står klar, ligesom andre dele af den regulatoriske infrastruktur fortsat mangler.
Som repræsentanter for den etablerede branche for medicinsk og diagnostisk udstyr i Danmark, bakker vi uforbeholdent op om den nye lovgivning, som formentlig vil sikre en generelt højere produktkvalitet og bidrage til øget patientsikkerhed på det diagnostiske område.
Alligevel er der behov for at tænde de røde advarselslamper, da rammerne for at implementere IVDR-lovgivningen endnu ikke er tilstrækkeligt på plads.
Overgangsregler er ikke nok
Implementeringsudfordringerne omkring IVDR-forordningen har med god grund skabt røre blandt mange af de virksomheder, der lever af at udvikle de bedste diagnostiske løsninger til sundhedsvæsenerne i Europa.
Desværre løser den blødere implementeringsmodel af IVDR, som blev vedtaget tidligere på året efter pres fra branchen, ikke manglen på de bemyndigede organer, men bidrager alene til, at eksisterende produkter kan blive noget længere tid på markedet.
Det nuværende set-up for IVDR-forordningen risikerer at gå stik imod intentionen om at højne patientsikkerheden
Henrik Christensen, Lene Laursen og Katrina Feilberg Schouenborg
Hhv. formand, DiaLab, vicedirektør, Medicoindustrien og markedschef, Dansk Erhverv
Og derfor står branchen fortsat tilbage med en stor usikkerhed i forhold til nye produkter.
En langsommelig proces vil ikke kun være en alvorlig udfordring for mange danske aktører på markedet for diagnostisk udstyr, der potentielt kan blive nødt til at kigge mod USA, når nye produkter skal lanceres, men vil også kunne medføre bølgeskvulp langt ind i sundhedsvæsenerne, fordi man ikke kan få de nye produkter, der er behov for. Eller sagt på en anden måde: Vi kan stå tilbage med et stivnet, ikke-innovativt europæisk marked for diagnostiske test de næste mange år.
Det nuværende set-up for implementeringen af IVDR-forordningen risikerer således at gå stik imod intentionen om at højne patientsikkerheden, som netop er kernen i IVDR.
Og det kan ingen være tjent med.
Derfor er det afgørende, at både danske og europæiske myndigheder i de kommende uger og måneder for alvor tager kapacitetsudfordringerne alvorligt og aktivt arbejder for at sikre den bedst mulige markedsadgang for såvel eksisterende som nye diagnostiske produkter, så vi hurtigt og effektivt kan komme i mål med godkendelserne efter IVDR.
Indsigt

 Louise Brown spørger Sophie LøhdeHvorfor er reglerne ikke ændret, så onlineplatforme kan levere håndkøbsmedicin?
Louise Brown spørger Sophie LøhdeHvorfor er reglerne ikke ændret, så onlineplatforme kan levere håndkøbsmedicin?
 Per Larsen spørger Sophie LøhdeHvad har regeringen gjort for børn og unge med svær overvægt?
Per Larsen spørger Sophie LøhdeHvad har regeringen gjort for børn og unge med svær overvægt?
 Karin Liltorp spørger Sophie LøhdeHvornår bliver retningslinjerne for udtrapning af antidepressiv medicin revideret?
Karin Liltorp spørger Sophie LøhdeHvornår bliver retningslinjerne for udtrapning af antidepressiv medicin revideret?
- Overblik: Her er den foreslåede VLAK-regerings politiske grundlag
- Kommuner og regioner vil presse mål for børns trivsel ind i regeringsgrundlag
- Medicinudgifterne stiger og stiger – men hullet i regionernes budgetter bliver ikke større
- Kommunernes budget eksploderer på det mest betændte område. Men Christiansborg stikker hovedet i busken
- Se kandidaterne til Lægeforeningens formandspost