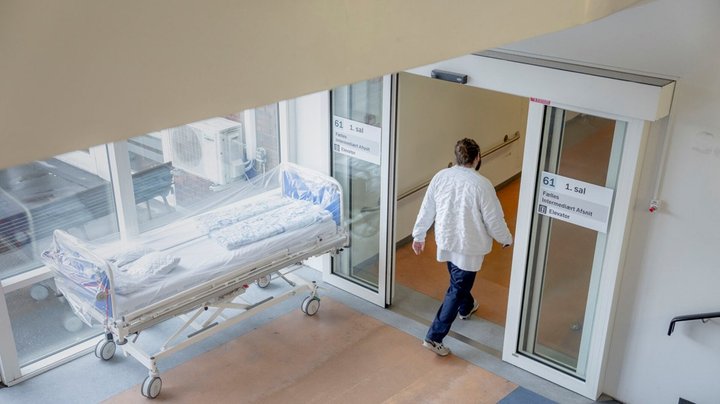
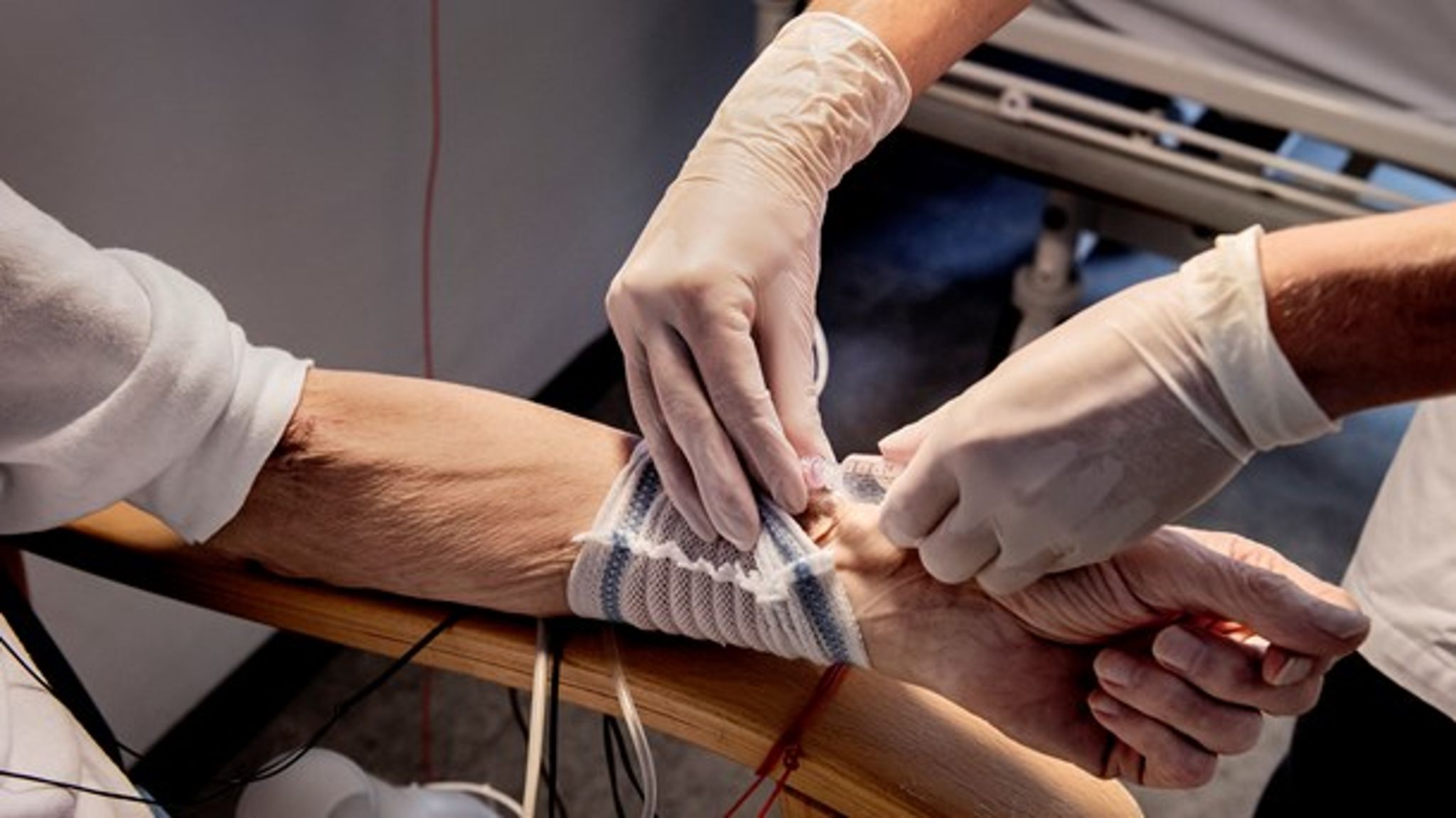
Forælder: Medicinrådets metoder medfører skæve konklusioner
Af Jens-Jacob Simonsen
Far til datter med Lebers, der potentielt kan behandles med Luxturna
Medicinrådets beslutning om behandlingen med genpræparatet Luxturna bør udfordres.
I debatindlægget 'Medicinrådets regneregler skal opdateres' følger sundhedsøkonom Lars Holger Ehlers op på min kritik af Medicinrådets manglende indregning af konsekvenserne for offentlige finanser og samfundsøkonomien ved at behandle – eller ikke behandle – børn og unge med alvorlig sygdom.
Sundhedsøkonomen er enig og skriver endda, at regnemetoderne hurtigst bør inkludere langsigtede beregninger af arbejdsmarkedsforhold og transfereringer såsom sygedagpenge og kontanthjælp ved en ny ansøgning om standardgodkendelse af Luxturna, som kan forhindre, at børn og unge med den særlige gendefekt Lebers bliver blinde.
Alle indlæg hos Altinget skal overholde de presseetiske regler.
Debatindlæg kan sendes til debat@altinget.dk.
Min 16-årige datter har Lebers, og jeg udfordrer derfor Medicinrådets beslutning om ikke at anbefale Luxturna, der er bedømt til at have vigtig merværdi, fordi prisen ifølge rådet er meget høj.
Principper mangler operationel substans
Medicinrådet blev etableret i 2017 for at skabe armslængde til politikerne ved prioriteringer på medicinområdet og for at dæmpe væksten i offentlige medicinudgifter.
Min tese er, at Medicinrådet har villet signalere til medicinalindustrien, at Danmark tør at sige nej til banebrydende, dyr behandling.
Jens-Jacob Simonsen
Far til datter med Lebers, der potentielt kan behandles med Luxturna
Der er bred politisk opbakning til armslængdeprincippet. Mulighederne for at søge aktindsigt i rådets overvejelser er minimale, og institutionen deltager sjældent i den offentlige debat om egne sager.
Medicinrådet opererer efter syv luftige og delvist modstridende folketingsprincipper, der kan suppleres med to tillægsprincipper om alvorlighed og økonomisk forsigtighed.
Princippernes foreningsmængde er blottet for operationel substans. Jeg vil i stedet sammenfatte rådets tre hovedopgaver:
Videnskabelig vurdering af evidens for og effekten af nye præparater, prisforhandling med medicinalindustrien og prioritering af den samlede ramme afsat til medicinaludgifter.
Jeg vil afsluttende anvende hovedopgaverne til at præsentere en provokerende forklaring på Medicinrådets konklusion om Luxturna.
Metoder indregner ikke samfundsøkonomi
Lars Holger Ehlers anfægter, at Medicinrådet i Luxturna-sagen ikke indregner økonomiske konsekvenser ved, at børn og unge forventeligt i høj grad forbliver selvhjulpne og selvforsørgende, hvis de behandles med Luxturna og derfor ikke – eller meget senere – bliver blinde.
Grundlaget for den særegne regnemetode er angiveligt et lighedsprincip og et hensyn om simple beslutningskriterier for at begrænse trækket på den administrative kapacitet.
For hensynet om administration vil jeg indvende, at medicinalvirksomheder kan levere de simple beregninger. Det forekommer også uetisk, hvis hensynet om en let administration vægter over hensynet til samfundsmæssige beslutninger om patienters førlighed og fremtid.
For lighedsprincippet er argumentet også problematisk. Ingen vil vel argumentere for, at samfundsøkonomiske gevinster bør være nødvendige for at godkende en behandling. Det kan ikke trække ned i vurderingen af andre behandlinger, at gevinsterne indregnes, hvor det er relevant.
Sagt på en anden måde: Hvis de samfundsøkonomiske gevinster og forbedret livskvalitet ved en behandling er tilstrækkelige til at gøre behandlingen meningsfyldt, hvori består lighedsbetragtningen ved at sige nej?
Medmindre udgangspunktet er et fast medicinbudget aftalt med Finansministeriet, hvor alle behandlinger konkurrerer om de samme midler, men det firkantede argument holder heller ikke vand.
Britisk strategi bør inspirere
For det første bør Medicinrådets opgave være at søge en udvidelse af det samlede medicinbudget, når nye banebrydende behandlinger kommer på områder uden tidligere behandlingsmuligheder.
Ellers giver vi afkald på at sikre et moderne og teknologisk opdateret offentligt sygehusvæsen, hvilket ikke kan være meningen.
For det andet bør Medicinrådets løbende arbejde være at optimere medicinbudgettet. Det kan ske ved indgåelse af nye prisaftaler på eksisterende produkter og ved at presse på for skift til billigere præparater med samme effekt.
Det svarer til briternes Nice-strategi om at skabe plads i medicinbudgettet til nye banebrydende præparater gennem "smart deals".
Endelig kunne man, hvis midlerne til engangsudgifterne til Luxturna ikke kan findes andre steder, finde delfinansiering til behandlingen i udlandet – i overensstemmelse med Sundhedsstyrelsens anbefalinger for sjældne sygdomme – ved at reducere Rigshospitalets øjenafdeling, som behovet bliver mindre for uden Luxturna-behandlingen i Danmark.
Internationale parter vurderer forskelligt
Medicinrådet har primært anvendt Grade-metoden, som indbefatter effekt, evidens og pris, til at vurdere ny medicin og har vurderet, at evidensen for Luxturnas effekt er lav.
Det er værd at se på, hvordan andre har vurderet evidensen:
| Medicinrådet (Danmark) | Federal Drug Administration (USA) | Det Europæiske Lægemiddelagentur (EU) | The National Institute for Health and Care Excellence (Storbritannien) |
| ”Evidensens kvalitet er meget lav.” |
”Alt i alt er der klare beviser for en klinisk nytteværdi, som er baseret på data fra det ene dækkende og gennemkontrollerede studie.” ”Et andet forsøg er ikke nødvendigt for at bekræfte virkningen på grund af den høje virkningsgrad og de robuste analyser.” |
”Virkningen bliver opretholdt i op til tre år.” ”Langtidseffekten fra tre år efter eksponering for Luxturna er endnu ikke blevet dokumenteret, og derfor bør effektmålinger registrere fra tre år efter eksponeringen for at kunne underbygge, at den kliniske effekt af det pågældende produkt varer ved.” ”Den lille population på kun 41 individer, som er blevet eksponeret, og hvoraf de fleste kun er blevet fulgt i tre år, betyder uundgåeligt, at viden om uhensigtsmæssige effekter er meget begrænset. Det kan dæmmes op ved, at hver person indgår i et 15-årigt opfølgningsprogram.” |
”Komiteen vidste, at undersøgelsesresultaterne tyder på vedvarende forbedring af synet i op til syv og et halvt år. Men den bed imidlertid mærke i, at meget få patienter i studiet havde taget den godkendte dosis af voretigene neparvovec (flere tog mindre doser), og at udvælgelseskriteriet ikke krævede, at de havde tilstrækkelige levedygtige nethindeceller i overensstemmelse med markedsføringstilladelsen.” ”Komiteen bemærkede, at voretigene neparvovec sandsynligvis ville give langsigtede fordele, selvom det var forbundet med betydelig usikkerhed.” ”De kliniske eksperter forklarede, at en langtidsbehandlingseffekt med voretigene neparvovec er biologisk plausibel og er deres forventning.” |
Sundhedsstyrelsen anbefaler for sjældne sygdomme en pragmatisk og fleksibel tilgang til udfordringerne ved fremskaffelse af traditionel evidens for behandlingseffekten af nye genetiske behandlingsmuligheder:
En bredde af videnskabelige metoder og tilgange inddrages, international best-practice og inspiration fra international kommunikation og samarbejde med ekspertcentre anvendes, og der henvises til forskningsmæssig behandling i udlandet, når muligheden er relevant.
Tabellen og anbefalingerne taler for sig selv, og desuden har institutionernes vurderinger ikke den samme faglige troværdighed.
I en sammenvejning vil Medicinrådets vurdering få en lav faktor, fordi institutionen er relativt ny i et lille land og næppe har afgørende nye oplysninger.
Selvfølgelig må evidensen for den langsigtede effekt af banebrydende genterapi for en sjælden sygdom være usikker. Men tabellen viser, at det ikke gør evidensen lav.
Med usikkerhed er der risiko for at begå to fejltyper. Vi risikerer at behandle for bagefter at se, at behandlingen ikke holdt så længe som forventet. Vi risikerer også ikke at behandle for bagefter at se, at behandlingen kunne have reddet patienternes syn.
Den sidste fejltype har en væsentlig omkostning, men den dækkes af andre offentlige finanser end medicinbudgettet – og af patienterne.
Pres på industrien får konsekvenser
Sundhedsøkonom Jes Søgaard, som jeg har drøftet Luxturna-sagen med, har argumenteret for, at medicinalindustrien bør fremlægge bedre evidens.
Jeg vil advare mod at presse medicinalindustrien for meget med øgede evidenskrav. Omkostningerne til forhandling og dokumentation til Det Europæiske Lægemiddelagentur og EU-landes sundhedsmyndigheder er skyhøje, hvilket påvirker priserne.
Danmark bør i stedet læne sig op ad andre troværdige lægemiddelagenturers vurderinger.
Det kan være vanskeligt at forstå Medicinrådets metodetilgang og konklusion, og jeg vil fremsætte en provokerende og foruroligende tolkning ud fra rådsformand Steen Werner Hansens udsagn om, at "Luxturna er den første genterapi, vi vurderer, og derfor lægges prisniveauet for lignende behandlinger, der omfatter mange flere patienter. Derfor har denne sag stor betydning".
Min tese er, at Medicinrådet har villet signalere til medicinalindustrien, at Danmark tør at sige nej til banebrydende, dyr behandling. Det har formet konklusionen og vurderingen af evidens og effekter.
Formålet kan være, at Danmark ikke længere skal være blandt de første europæiske lande, som tager nye behandlinger i brug og betaler de højeste priser. Formålet kan også være at teste politikernes opbakning til armslængdeprincippet.
Hvis det er forklaringen, er Lebers-patienterne ilde stedt, fordi ingen rationelle argumenter for effekter kan ændre på afgørelsen.
Kræver flere småjusteringer
Afslutningsvist vil jeg skitsere mulige småjusteringer i Medicinrådets metoder:
Samfundsøkonomiske og offentligt økonomiske konsekvensberegninger inddrages fremover i relevante effektvurderinger. Ved overgangen til Qaly-vurdering i slutningen af 2020 kan de eventuelt indarbejdes i Qaly, selvom det reducerer transparensen.
Danmark er en lille indkøber af præparater for sjældne sygdomme, og der søges at få etableret fælles indkøbsaftaler med eksempelvis de nordiske lande. Alternativt følger Danmark trop, når store europæiske indkøbere indgår aftaler, i erkendelse af at Danmarks forhandlingsrum er begrænset.
Vurderingen af effekt og evidens holdes fortrolige, indtil prisforhandlingerne er afsluttede.
Stillingtagen til nye behandlinger for sjældne sygdomme uden noget alternativ sker efter politiske konsultationer, som kan påvirke rammen til medicinudgifter.
Der arbejdes efter britisk forbillede med at indgå "smart deals" på eksisterende præparater.
Der skabes øget transparens om de behandlingstyper og omkostningsniveauer, som det offentlige sundhedssystem fremover ikke forventes at dække, så der kan suppleres med private sundhedsforsikringer.
Indsigt
 Henrik Thorup80 år
Henrik Thorup80 årI dag
Fhv. formand for statsrevisorerne og regionsrådsmedlem (DF), Region Hovedstaden Morten Jensen53 år
Morten Jensen53 årI dag
Leder, Center for Misbrug & Udsatte, Esbjerg Kommune, enhedschef, Institution Vadehavet, Kriminalforsorgen Thea Kølsen Fischer59 år
Thea Kølsen Fischer59 årI dag
Forskningschef og ledende overlæge, Nordsjællands Hospital, klinisk professor, Københavns Universitet, fhv. overlæge, Statens Serum Institut

 Louise Brown spørger Sophie LøhdeHvorfor er reglerne ikke ændret, så onlineplatforme kan levere håndkøbsmedicin?
Louise Brown spørger Sophie LøhdeHvorfor er reglerne ikke ændret, så onlineplatforme kan levere håndkøbsmedicin?
 Per Larsen spørger Sophie LøhdeHvad har regeringen gjort for børn og unge med svær overvægt?
Per Larsen spørger Sophie LøhdeHvad har regeringen gjort for børn og unge med svær overvægt?
 Karin Liltorp spørger Sophie LøhdeHvornår bliver retningslinjerne for udtrapning af antidepressiv medicin revideret?
Karin Liltorp spørger Sophie LøhdeHvornår bliver retningslinjerne for udtrapning af antidepressiv medicin revideret?
- Her er tre ministerier, den nye regering bør slå sammen
- Foreninger: Det er ikke længere nok at behandle adhd og autisme som et psykiatrisk spørgsmål
- Her holder politikerne tale grundlovsdag 2026
- JP/Politikens Hus indstifter ny demokratipris
- Camilla Rathcke til KL og Danske Regioner: Sådan kan vi styrke børne- og ungepsykiatrien sammen