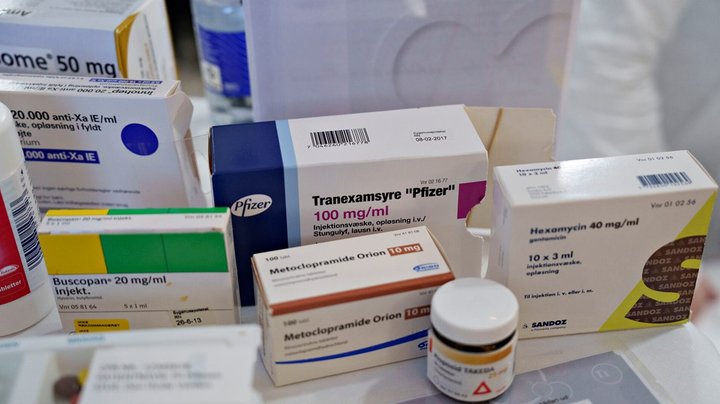
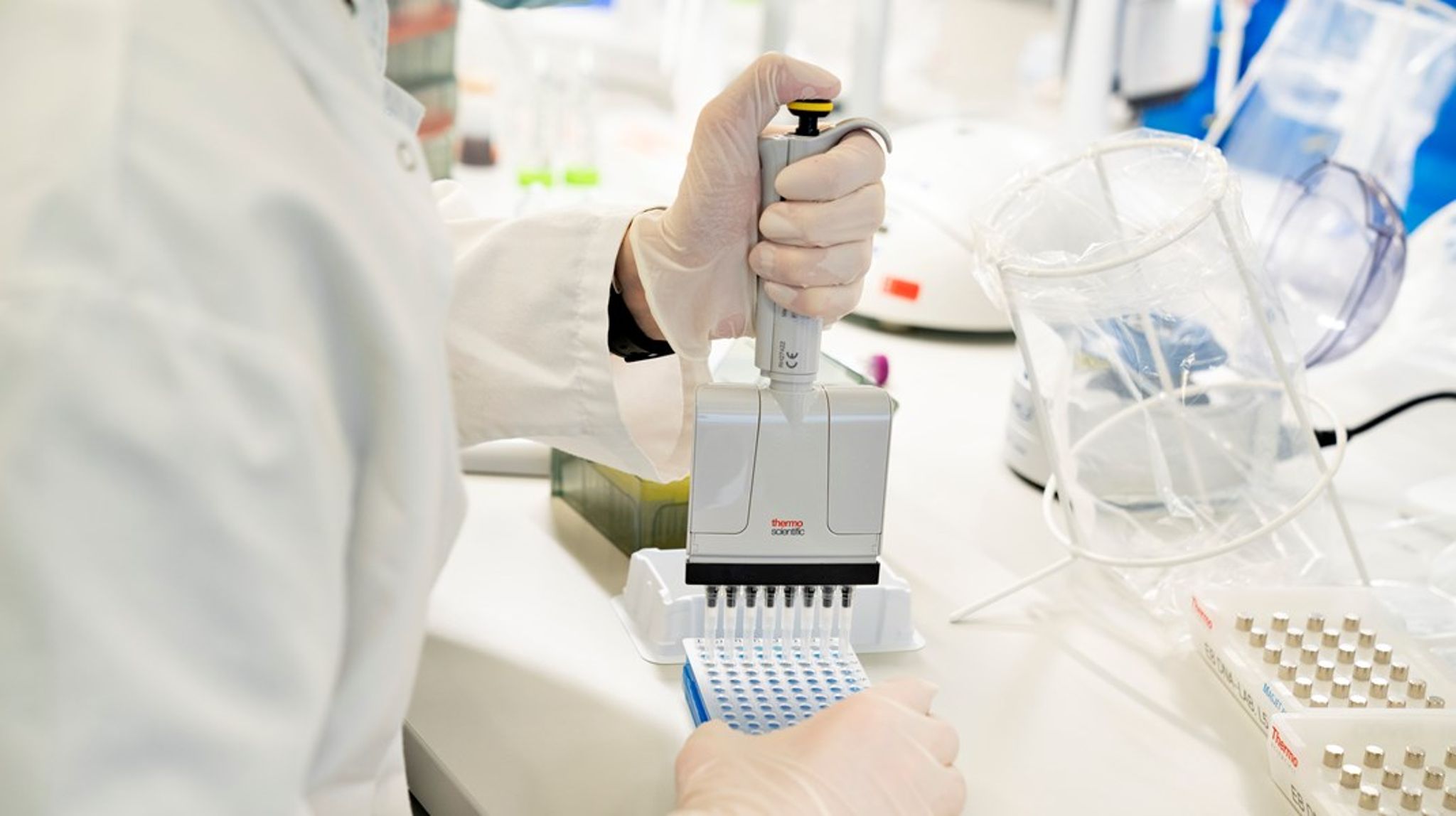
M-profiler og sundhedsaktører: Danskere med sjældne sygdomme kan snart blive nødt til at rejse til Kina
Stine Bosse, Rosa Eriksen, René Mathiasen m.fl. (se alle afsendere i faktaboks)
Vi fremhæver ofte med rette vores stærke sundhedsvæsener og velfærdsstater i Europa.
Men en hurtig og ordentlig behandling er ikke længere nogen selvfølge. Vi er i nemlig i færd med at overlade feltet til Kina og USA.
På bare ti år er Europas globale andel af de kommercielle kliniske forsøg halveret fra 18 til 9 procent. I samme periode har Kina fordoblet sin andel til 18 procent, mens USA fortsat er i førertrøjen.
Det betyder, at omkring 60.000 færre patienter i EU deltager i kliniske forsøg. Danmark har ellers været blandt de førende i Europa, men også her er udviklingen ved at vende.
Kina er forbi Europa
Kina og USA har store, samlede markeder både for lægemidler og for kliniske forsøg. Det giver dem en klar fordel. Kina har allerede overhalet Europa i klinisk forsøgsaktivitet – og det mærkes direkte af patienterne.
Danske kræftpatienter og patienter med sjældne sygdomme har i dag færre behandlingsmuligheder end i Tyskland, som til gengæld ligger bagefter USA. Hvis vi ikke handler, kommer vi endnu længere bagud.
Stine Bosse, Næstformand af Europa-Parlamentets sundhedsudvalg (M)
Rosa Eriksen, sundhedsordfører, (M)
René Mathiasen, formand, DanPedMed, overlæge, klinisk lektor, Afdeling for Børn og Unge, Rigshospitalet
Kjeld Schmiegelow, professor, BørneUngeKlinikken, Rigshospitalet
Lars Østergaard, cheflæge, Infektionssygdomme, Aarhus Universitetshospital og professor, Klinisk Institut på Aarhus Universitet
Sebastian Honoré, stifter, Cure Lowe Foundation og far til Walther, der lever med en sjælden sygdom
Jan Brink Valentin, senior statistiker, Dansk Center for Sundhedstjenesteforskning, Klinisk institut, Aalborg Universitet, FU medlem i Sjældne Diagnoser
Liselotte Wesley Andersen, Forperson Sjældne Diagnoser, pensioneret seniorforsker, Ph.D. Cand. Scient.
En væsentlig årsag er EU's fragmenterede regelsæt. Hvert EU-land (og nogle gange også regionerne) har sine egne etik-komiteer og processer, og der findes ingen fælles europæisk model.
Resultatet er færre forsøg, langsommere adgang til nye behandlinger, risiko for tab af kompetencer i sundhedsvæsnet og mindre innovation. USA styrker sin førerposition, Kina rykker frem – og Europa mister terræn.
For patienter med sjældne diagnoser kan et klinisk forsøg være den eneste mulighed for at få adgang til en ny behandling – flere år før den rammer markedet. Men Europas andel af disse behandlinger er faldet dramatisk.
Europa taber terræn
Hvor Europa og EU for 15 år siden var en førende inden for ATMP’er, både hvad angår udvikling, godkendelse og regulering, er vi nu faldet af og har opgivet førerpositionen til USA.
Klinisk forskning skaber værdi her og nu. Den giver patienter adgang til nye behandlinger, løfter kompetencer hos læger og sygeplejersker, styrker rekruttering og skaber vækst. Virksomheder, der forsker i Europa, producerer og lancerer typisk også deres lægemidler her.
EU har ellers en ti år gammel forordning om kliniske forsøg, der skulle styrke Europas konkurrenceevne på området, men forskelle mellem landene og lange procedurer gør, at vi taber terræn.
I USA kan et forsøg godkendes på 30 dage eller mere – i EU kan det tage fra 60 til 106 dage.
Derfor skal vi handle nu. Europa-Kommissionens nye strategi Choose Europe for Life Sciences, som skal få globale virksomheder at vælge netop Europa, er et vigtigt skridt på vejen. Men den kræver konkrete initiativer, ikke mindst på området kliniske forsøg.
Derfor foreslår vi konkrete tiltag, der kan gøre en stor forskel i EU, både for vores patienter og for at opbygning af et europæisk lederskab indenfor forskning og produktion af nye, banebrydende behandlinger.
Hurtigere godkendelser i EU
Vores forslag:
Gør EU's godkendelsesproces for kliniske forsøg hurtigere, enklere og globalt konkurrencedygtig – til gavn for patienterne.
Koordiner og optimer: EU bør harmonisere den etiske vurdering på tværs af medlemsstater, så godkendelser sker hurtigere og mere effektivt.
En fælles europæisk ramme må dog ikke ende som et kompromis på laveste niveau. Europas styrke er de høje etiske standarder, der beskytter patienterne og sikrer tillid til forskningen.
For mennesker med for eksempel sjældne diagnoser, hvor der ofte ingen behandling findes, er villigheden til at deltage stor. Derfor skal vi sikre, at hurtigere processer ikke sker på bekostning af patientsikkerhed og etisk kvalitet.
EU bør harmonisere den etiske vurdering på tværs af medlemsstater, så godkendelser sker hurtigere og mere effektivt.
se alle afsendere i faktaboksen
Effektiviteten kan måles ved både kvantitet og kvalitet af spørgsmål fra nationale videnskabsetiske komiteer til sponsorer – det vil sige pharmavirksomhederne.
Etabler en fælles standard: Indfør en fælles europæisk godkendelsesprocedure, især inden for sjældne diagnoser og personlige mediciner (ATMP). I dag er det alt for dyrt, langsomt og kompliceret at arbejde på tværs af landegrænser med små patientgrupper.
Det bremser innovation, produktion og patientadgang til livsvigtige behandlinger – til skade for europæiske patienter med et akut behov for nye løsninger.
Etabler et fælles europæisk patientregister som inkluderer diagnosekoder for sjældne sygdomme, således at centre med høj forekomst af pågældende sygdom kan identificeres via autoriserede forskningscentre og dermed gøre rekrutteringen til kliniske forsøg mere målrettet.
Kort sagt: EU skal gå fra fragmenteret bureaukrati til én sammenhængende, konkurrencedygtig ramme, der accelererer forskning og sikrer hurtigere adgang til behandling.
Klinisk forskning er selve fundamentet for Europas konkurrenceevne i life science. Hvis vi ikke styrker rammerne nu, taber vi både innovation, arbejdspladser og vigtigst af alt – vores patienters mulighed for at få bedst mulig behandling. Også her i Danmark.
Indsigt
 Jes Bruun Lauritzen70 år
Jes Bruun Lauritzen70 årI dag
Klinisk professor, Institut for Klinisk Medicin, Københavns Universitet, overlæge, Ortopædkirurgisk afdeling, Bispebjerg Hospital Lene Brøndum Jensen52 år
Lene Brøndum Jensen52 årI dag
Afdelingschef, Afdeling for Sundhedsstruktur, Etik og Beredskab, Indenrigs- og Sundhedsministeriet Mette Wier65 år
Mette Wier65 årI dag
Direktør, professor, DTU Management, Institut for Teknologi, Ledelse og Økonomi, medlem af bestyrelsen for Gate21, Det Tekniske Universitetshospital og Danish Life Cycle Cluster

 Louise Brown spørger Sophie LøhdeHvorfor er reglerne ikke ændret, så onlineplatforme kan levere håndkøbsmedicin?
Louise Brown spørger Sophie LøhdeHvorfor er reglerne ikke ændret, så onlineplatforme kan levere håndkøbsmedicin?
 Per Larsen spørger Sophie LøhdeHvad har regeringen gjort for børn og unge med svær overvægt?
Per Larsen spørger Sophie LøhdeHvad har regeringen gjort for børn og unge med svær overvægt?
 Karin Liltorp spørger Sophie LøhdeHvornår bliver retningslinjerne for udtrapning af antidepressiv medicin revideret?
Karin Liltorp spørger Sophie LøhdeHvornår bliver retningslinjerne for udtrapning af antidepressiv medicin revideret?
- Overblik: Her er den foreslåede VLAK-regerings politiske grundlag
- Kommuner og regioner vil presse mål for børns trivsel ind i regeringsgrundlag
- Kommunernes budget eksploderer på det mest betændte område. Men Christiansborg stikker hovedet i busken
- Medicinudgifterne stiger og stiger – men hullet i regionernes budgetter bliver ikke større
- Se kandidaterne til Lægeforeningens formandspost